來源:網絡資源 2023-08-28 18:12:36
堿及堿的化學性質
堿由離子構成,堿在水溶液中能解離出金屬離子和氫氧根離子(OH-)。
常見的堿有氫氧化鈉(NaOH) 、氫氧化鈣 Ca(OH)₂、氨水(NH₃·H₂O)等。
1.氫氧化鈉、氫氧化鈣的物理性質、用途
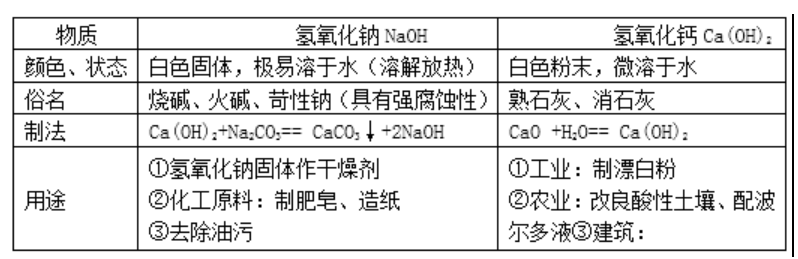
2.堿的化學性質
紫色石蕊試液遇堿溶液變藍,無色酚酞試液遇堿溶液變紅。
①酸性氧化物+堿→鹽+水
2NaOH+CO₂=Na₂CO₃+H₂O
*2NaOH+SiO₂=Na₂SiO₃+H₂O
Ca(OH)2+CO₂=CaCO₃↓+H₂O
②酸+堿→鹽+水(中和反應)
NaOH+HCl=NaCl+H₂O
Ca(OH)₂+H₂SO4=CaSO4+2H₂O
③*鹽+堿→新鹽+新堿(反應物均可溶)
2NaOH+CuSO4=Na₂SO4+Cu(OH)₂↓
編輯推薦:

歡迎使用手機、平板等移動設備訪問中考網,2025中考一路陪伴同行!>>點擊查看